- Autor Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:32.
- Ostatnio zmodyfikowany 2025-01-23 12:43.
Spektrofotometria to technika eksperymentalna stosowana do pomiaru stężenia substancji rozpuszczonej w określonym roztworze poprzez obliczenie ilości światła zaabsorbowanego przez tę substancję. Ta technika jest bardzo przydatna, ponieważ niektóre związki będą również absorbować różne długości fal światła o różnym natężeniu. Analizując światło przechodzące przez roztwór, możesz zidentyfikować związki rozpuszczone w roztworze i ich stężenia. Narzędziem wykorzystywanym do analizy roztworów tą techniką w laboratorium jest spektrofotometr.
Krok
Część 1 z 3: Przygotowanie próbki

Krok 1. Włącz spektrofotometr
Większość spektrofotometrów wymaga rozgrzania, zanim będą mogły dawać dokładne pomiary. Uruchom więc maszynę, a następnie pozostaw ją na co najmniej 15 minut przed pomiarem próbki.
Wykorzystaj ten czas na przygotowanie próbki

Krok 2. Wyczyść kuwetę lub probówkę
W laboratoriach szkolnych mogą być dostępne jednorazowe probówki, których nie trzeba najpierw czyścić. Jeśli jednak używasz zwykłej kuwety lub probówki, pamiętaj o dokładnym wyczyszczeniu aparatu przed użyciem. Wypłucz wszystkie kuwety wodą dejonizowaną.
- Zachowaj ostrożność podczas korzystania z kuwet, ponieważ są one dość drogie.
- Podczas używania kuwety nie należy dotykać strony, po której przechodzi światło (zwykle przezroczystej strony pojemnika).
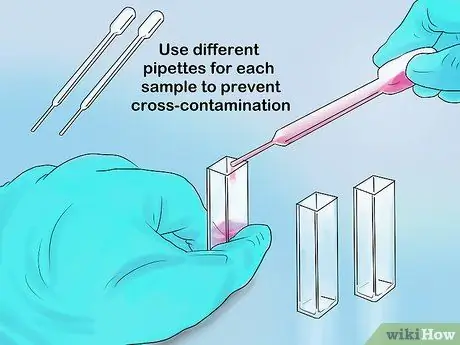
Krok 3. Wlej wystarczającą ilość próbki do kuwety
Maksymalna objętość części kuwety to 1 ml, natomiast maksymalna objętość probówki to 5 ml. Twoje pomiary powinny być dokładne, o ile światło spektrofotometru może nadal przechodzić przez próbkę, a nie przez pustą część pojemnika.
Jeśli używasz pipety do wprowadzania próbek, użyj nowej końcówki dla każdej próbki. W ten sposób można uniknąć zanieczyszczenia krzyżowego

Krok 4. Przygotuj roztwór kontrolny
Te roztwory, znane również jako ślepe próby lub ślepe próby, zawierają tylko rozpuszczalnik w analizowanym roztworze. Na przykład, jeśli masz próbkę soli rozpuszczonej w wodzie, ślepym roztworem, którego potrzebujesz, jest woda. Jeśli woda, której używasz, jest czerwona, powinieneś również użyć czerwonego roztworu ślepej próby. Użyj podobnego pojemnika do przechowywania roztworu ślepego w tej samej objętości co próbka.

Krok 5. Wytrzyj zewnętrzną stronę kuwety
Przed włożeniem kuwety do spektrofotometru należy upewnić się, że jest ona czysta, aby uniknąć zakłóceń pomiarów spowodowanych cząsteczkami kurzu lub zanieczyszczeniami. Użyj niestrzępiącej się szmatki, aby usunąć wszelkie krople wody lub kurz przylegające na zewnątrz kuwety.
Część 2 z 3: Eksperymentowanie

Krok 1. Określ i dostosuj długość fali światła do analizy próbki
Użyj pojedynczej długości fali światła (wiązka monochromatyczna), aby zwiększyć skuteczność pomiaru. Wybierz kolor światła, który może zostać pochłonięty przez zawartość chemiczną, która, jak się sądzi, jest rozpuszczona w badanej próbce. Ustaw długość fali zgodnie ze specyfikacją używanego spektrofotometru.
- W laboratoriach szkolnych te długości fal są zwykle podawane w instrukcjach doświadczalnych.
- Ponieważ próbka odbija całe światło widzialne, długość fali koloru światła eksperymentalnego jest zwykle zawsze inna niż kolor próbki.
- Obiekt ma określony kolor, ponieważ odbija określoną długość fali i pochłania wszystkie inne kolory. Trawa wydaje się zielona, ponieważ zawarty w niej chlorofil odbija zieleń i pochłania inne kolory.
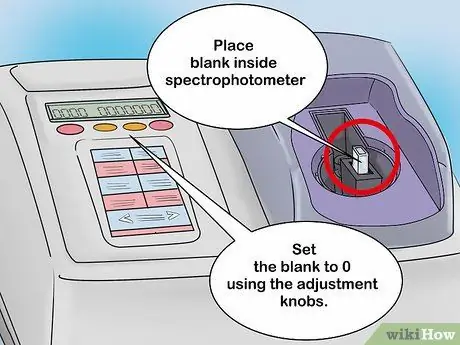
Krok 2. Skalibruj spektrofotometr ślepą próbą
Umieścić roztwór ślepy w uchwycie kuwety i zamknąć spektrofotometr. Na ekranie spektrofotometru analogowego znajduje się igła, która porusza się w zależności od intensywności wykrywania światła. Po włożeniu pustego roztworu igła powinna przesunąć się w prawo. Zapisz tę wartość na wypadek, gdyby była potrzebna później. Pozostaw roztwór do próby ślepej w spektrofotometrze, a następnie przesuń igłę do zera za pomocą pokrętła regulacyjnego.
- W ten sam sposób można również kalibrować spektrofotometry cyfrowe. Jednak to narzędzie jest wyposażone w cyfrowy ekran. Ustawić odczyt ślepej próby na 0 za pomocą pokrętła kontrolnego.
- Nawet jeśli roztwór ślepy zostanie usunięty ze spektrofotometru, kalibracja będzie nadal ważna. Tak więc, kiedy mierzysz całą próbkę, absorbancja ślepej próby zostanie automatycznie zmniejszona.

Krok 3. Usuń ślepą próbę i przetestuj wyniki kalibracji spektrofotometru
Nawet po wyjęciu roztworu próby ślepej ze spektrofotometru igła lub numer na ekranie powinny nadal wskazywać 0. Włóż roztwór próby ślepej z powrotem do spektrofotometru i upewnij się, że odczyt się nie zmienia. Jeśli spektrofotometr jest prawidłowo skalibrowany przy użyciu roztworu ślepego, wynik na ekranie powinien nadal wynosić 0.
- Jeśli igła lub liczba na ekranie nie wskazuje 0, powtórz kroki kalibracji z roztworem ślepym.
- Jeśli problem nie ustąpi, poszukaj pomocy lub poproś kogoś o sprawdzenie spektrofotometru.

Krok 4. Zmierz absorbancję próbki
Usuń ślepą próbę i włóż próbkę do spektrofotometru. Odczekaj około 10 sekund, aż wskazówki się ustabilizują lub cyfry na wyświetlaczu cyfrowym przestaną się zmieniać. Zapisz procent transmitancji i/lub absorbancji próbki.
- Im więcej światła zostanie przepuszczone, tym mniej światła zostanie pochłonięte. Zazwyczaj należy zapisać wartość absorbancji próbki, która jest zazwyczaj wyrażona jako liczba dziesiętna, na przykład 0,43.
- Powtórz pomiar każdej próbki co najmniej trzy razy, a następnie oblicz średnią. W ten sposób uzyskane wyniki będą dokładniejsze.

Krok 5. Powtórz eksperyment z różnymi długościami fal światła
Twoja próbka może zawierać kilka związków o różnej absorbancji w zależności od długości fali światła. Aby zmniejszyć niepewność, powtórz pomiary próbek w odstępach długości fali 25 nm w całym spektrum światła. W ten sposób można wykryć w próbce inne rozpuszczone chemikalia.
Część 3 z 3: Analiza danych absorbancji

Krok 1. Oblicz transmitancję i absorbancję próbki
Przepuszczalność to ilość światła, które może przejść przez próbkę i dotrzeć do spektrofotometru. Tymczasem absorbancja to ilość światła pochłaniana przez jedną z rozpuszczonych substancji chemicznych w próbce. Istnieje wiele nowoczesnych spektrofotometrów dających wynik w postaci transmitancji i absorbancji. Jeśli jednak uzyskasz wartość natężenia światła, możesz również samodzielnie obliczyć te dwie wartości.
- Przepuszczalność (T) można określić, dzieląc natężenie światła przechodzącego przez roztwór próbki przez ilość światła przechodzącego przez roztwór ślepy. Ta wartość jest zwykle wyrażana jako liczba dziesiętna lub procent. T = I/I0, gdzie I jest intensywnością próbki, a I0 to intensywność blanku.
- Absorbancja (A) jest wyrażana jako ujemna transmitancja logarytmu o podstawie 10 (wykładnik): A = -log10T. Czyli, jeśli T = 0, 1, A = 1 (0, 1 to 10 do potęgi -1). Oznacza to, że 10% światła przechodzi, a 90% jest pochłaniane. Tymczasem, jeśli T= 0,01, A = 2 (0,01 to 10 do potęgi -2). Oznacza to, że przepuszczane światło wynosi 0,1%.
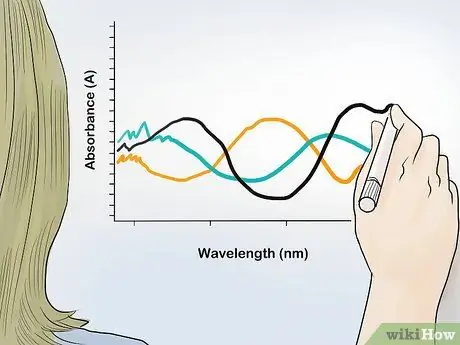
Krok 2. Wykreśl wykres wartości absorbancji w funkcji długości fali
Wyraź wartość absorbancji jako oś y, a długość fali jako oś x. Z kropek wszystkich wyników absorbancji dla każdej długości fali otrzymasz widmo absorbancji próbki i zidentyfikujesz zawartość związku i jego stosunek w próbce.
Widma absorbancji zwykle mają piki przy pewnych długościach fal. Te szczytowe długości fal pozwalają zidentyfikować określone związki
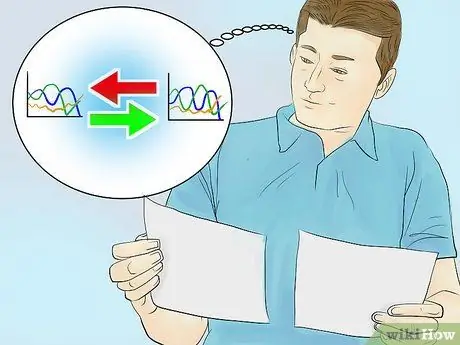
Krok 3. Porównaj swoje widmo absorbancji z wykresem znanego związku
Każdy związek ma unikalne widmo absorbancji i zawsze ma tę samą szczytową długość fali w każdym pomiarze. Porównując otrzymany wykres z wykresem pewnego znanego związku, możesz zidentyfikować zawartość substancji rozpuszczonej w roztworze próbki.






